Documenti esaminati:
26 ottobre 2023 Wilkinson et al – Un modello standardizzato della Brighton Collaboration con considerazioni chiave per una valutazione del rapporto beneficio/rischio per il vaccino Novavax COVID-19 (NVX-CoV2373), un vaccino proteico ricombinante con adiuvante Matrix-M per prevenire la malattia causata dai virus SARS-CoV-2
- 18 ottobre 2023 – Aggiornamento COVID-19: nuova formulazione del vaccino Novavax per il periodo 2023-2024
- Giugno 2023 Smith et al – Sicurezza del vaccino NVX-CoV2373 COVID-19 in studi clinici randomizzati controllati con placebo
- Febbraio 2023 Saint-Gerons et al – Miopericardite associata al vaccino Novavax COVID-19 (NVX-CoV2373): un'analisi retrospettiva dei rapporti sulla sicurezza dei singoli casi da VigiBase
- Dicembre 2022 Ahmad et al – Miopericardite conseguente sia a BNT162b2 che a NVX-CoV2373
7 giugno 2022 – Food and Drug Administration statunitense. Documento informativo VRBPAC sul vaccino Novavax COVID-19 (NVX-CoV2373). Aggiornato 2022
26 ottobre 2023 Wilkinson et al – Un modello standardizzato della Brighton Collaboration con considerazioni chiave per una valutazione del rapporto beneficio/rischio per il vaccino Novavax COVID-19 (NVX-CoV2373), un vaccino proteico ricombinante con adiuvante Matrix-M per prevenire la malattia causata dai virus SARS-CoV-2.
- “Novavax, Inc. ha sviluppato un vaccino proteico ricombinante formulato con l’ adiuvante Matrix-M™ a base di saponina (denominato NVX-CoV2373) contro SARS-CoV-2”
- “ La nanoparticella ricombinante del picco SARS-CoV-2 (rS) è costituita da una proteina altamente purificata costruita a partire dal picco SARS-CoV-2 di tipo selvaggio a lunghezza intera. Questa proteina si basa sulla sequenza del gene spike del ceppo originale Wuhan-Hu-1 ed è prodotta utilizzando un sistema di espressione di baculovirus in una linea cellulare di insetti derivata da cellule Sf9 della specie Spodoptera frugiperda ”
- “In particolare , la flessibilità di questa fase consente l’ uso di costrutti genetici alternativi secondo necessità , come le proteine S delle nuove varianti SARS-CoV-2”
- "la proteina ricombinante del picco è stata modificata per contenere sostituzioni di aminoacidi nella scissione della furina S1/S2 e due sostituzioni di prolina nel dominio S2 per conferire resistenza alla proteasi e produrre una conformazione prefusione stabile"
- “ il baculovirus ricombinante viene replicato nelle cellule Sf9 e il gene del picco NVX-CoV2373 viene trascritto, tradotto e modificato post-traduzionalmente (cioè glicosilato), determinando una produzione ad alto rendimento della proteina S ricombinante SARS-CoV-2 in un nativo conformazione trimero. Successivamente, i trimeri vengono raccolti, purificati mediante cromatografia su colonna e filtrazione e dializzati in una soluzione tampone contenente detergente in cui si autoassemblano in particelle di circa 60 nanometri disposte attorno a un nucleo di polisorbato 80 .
- Nella fase finale, le nanoparticelle di proteina S vengono formulate con l'adiuvante a base di saponina Matrix-M (Matrix-M TM )
- “ La formulazione con Matrix-M, un adiuvante potente e stabile studiato su oltre 37.000 individui, consente di risparmiare la dose di antigene e di migliorare le risposte immunitarie mantenendo un profilo di sicurezza favorevole”
- In oltre 40 paesi, NVX-CoV2373 è autorizzato per l'uso in caso di emergenza o ha ricevuto la piena approvazione
- SICUREZZA: “La sicurezza di NVX-CoV2373 è stata valutata durante i programmi completi di sviluppo clinico e non clinico e nella sorveglianza della sicurezza post-autorizzazione. Non sono stati identificati rischi nel programma di sviluppo preclinico mentre i dati supportavano la dose e il regime approvati per l’uso umano. Il profilo di sicurezza di NVX-CoV2373 indica che questo vaccino è ben tollerato, come dimostrato dai dati di oltre 31.000 partecipanti che hanno ricevuto NVX-CoV2373 in 5 studi clinici randomizzati controllati ”.
- Novavax = 5 ug (proteina del ceppo Wuhan) + 50 ug Matrix-M
- “le prove sulla longevità della risposta anticorpale all’infezione da COVID-19 sono scarse… pertanto, è possibile una reinfezione da COVID-19”
- L'adiuvante Matrix-M è prodotto miscelando estratti definiti e parzialmente purificati della corteccia dell'albero Quillaja saponaria Molina, denominati Frazione A e Frazione C, con colesterolo e fosfatidilcolina in presenza di un detergente.
- I complessi sferici immunostimolanti risultanti sono particelle di circa 40 nm di diametro, notevolmente stabili, tenute insieme dalla forte affinità tra saponina e colesterolo . La particella fornisce inoltre stabilità chimica alle fragili molecole di saponina in condizioni in cui le saponine libere si degradano rapidamente.
- La somministrazione adiuvante di Matrix-M è stata generalmente ben tollerata negli esseri umani e negli animali. I dati tossicologici provenienti da studi sugli animali per valutare l’adiuvante Matrix-M, da solo o in co-somministrazione con diversi antigeni vaccinali, non hanno dimostrato tossicità sistemiche o organo-specifiche rilevanti. Si sono verificate riduzioni transitorie e incoerenti del peso corporeo e dei parametri di massa dei globuli rossi
- Matrix-M è stato testato con vaccini nanoparticellari contro l’influenza, l’RSV e l’Ebola
- “Anche l’immunostimolazione con l’adiuvante Matrix-M può contribuire all’immunotossicità”
- studi sulla biodistribuzione di Matrix-M sono stati condotti nei roditori
- la biodistribuzione del picco di nanoparticelle non è stata eseguita – PERCHÉ? – “Prevediamo che il vaccino co-formulato seguirà un percorso convenzionale di traffico dell’antigene proteico dopo la somministrazione intramuscolare: l’antigene assorbito dalle cellule dendritiche migrerà al linfonodo drenante dove verrà elaborato e presentato alle cellule T dalle cellule presentanti l’antigene e avviare la risposta immunitaria. Pertanto, ci aspettiamo che la distribuzione dell’antigene rilevabile sia per lo più limitata ai linfonodi locali”
- Non sono stati condotti studi per misurare la persistenza nei tessuti locali o distali a causa delle dosi molto basse di microgrammi di antigene, sarà difficile rilevarlo nel siero e nei tessuti.
- la somministrazione nel contesto di un adiuvante della saponina è progettata per facilitare il trasporto ai linfonodi drenanti piuttosto che la formazione di un deposito locale.
- "Novavax prevede un basso potenziale di effetti indesiderati gravi e tossicità nei neonati, lattanti e bambini"
- "Novavax prevede un basso potenziale di effetti indesiderati gravi e tossicità nelle donne in gravidanza e nei feti"
- "Novavax non crede che esistano altre popolazioni speciali che sarebbero più suscettibili a gravi effetti indesiderati e tossicità"
18 ottobre 2023 – Aggiornamento COVID-19: nuova formulazione del vaccino Novavax per il 2023-2024.
- la formulazione originale del vaccino Novavax non è più autorizzata per l’uso negli Stati Uniti
- La formulazione 2023-2024 del vaccino Novavax contiene la proteina spike del ceppo XBB.1.5 Omicron di SARS-CoV-2.
- Non sono disponibili studi clinici che valutino la SICUREZZA o l’efficacia del vaccino Novavax 2023-2024
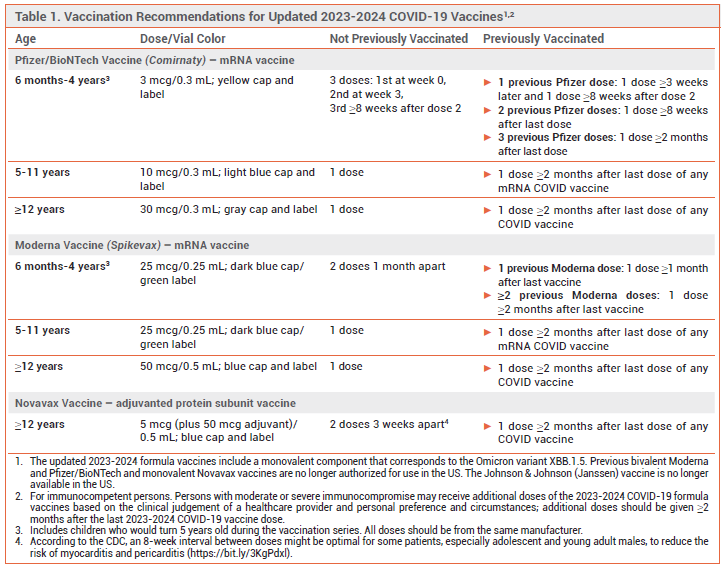
- “Il vaccino aggiornato Novavax COVID-19 è indicato per l’uso in persone di età ≥ 12 anni che non hanno già ricevuto un’altra formulazione del vaccino COVID-19 2023-2024”
- ATTENZIONE: “Chi non è stato precedentemente vaccinato contro il COVID-19 dovrebbe ricevere 2 dosi; l’etichettatura del prodotto raccomanda che vengano somministrati a 3 settimane di distanza l’uno dall’altro, ma secondo il CDC, un intervallo di 8 settimane tra le dosi potrebbe essere ottimale per alcuni pazienti (soprattutto adolescenti e giovani maschi adulti) per ridurre il rischio di miocardite e pericardite ”
Giugno 2023 Smith et al – Sicurezza del vaccino NVX-CoV2373 COVID-19 in uno studio clinico randomizzato controllato con placebo.
- 4 studi clinici con 30.058 che hanno ricevuto Novavax, 19.892 che hanno ricevuto placebo
- L’11,4% ha avuto una reazione sistemica di Grado 3+ entro 7 giorni (3,6% per il placebo)
- 21 decessi o 0,07% (12 decessi o 0,06% nel placebo)
- “ Gli eventi di grado 3-4 sono stati più frequenti nei soggetti che hanno ricevuto il vaccino rispetto a quelli che hanno ricevuto il placebo, il che non è inaspettato per un vaccino adiuvato rispetto a un placebo salino. I tassi di SAE riportati dai partecipanti che hanno ricevuto NVX-CoV2373 o placebo erano simili”
- “A seguito dell’autorizzazione all’immissione in commercio di NVX-CoV2373, sono pervenute segnalazioni di miocardite e pericardite da diverse regioni, tra cui l’Australia e l’Unione Europea . Sulla base di una revisione dei rapporti cumulativi post-autorizzazione, miocardite e pericardite sono ora considerate rischi identificati per NVX-CoV2373”
- “Non è chiaro quale meccanismo specifico causi l’infiammazione del tessuto cardiaco”.
Febbraio 2023 Saint-Gerons et al – Miopericardite associata al vaccino Novavax COVID-19 (NVX-CoV2373): un'analisi retrospettiva dei rapporti sulla sicurezza dei singoli casi da VigiBase.
- 61 segnalazioni di sicurezza per miocardite e pericardite segnalate alle autorità di regolamentazione, 24 gravi, 19 hanno richiesto il ricovero ospedaliero, 3 erano pericolose per la vita, 1 invalidante, nessuna fatale
- età media 36 anni, 62%, 38% donne
- Il 70% aveva dolore al petto
- periodo mediano con insorgenza 3 giorni dopo il jab
- solo il 13% si è ripreso
- “È stato riscontrato un segnale di sproporzionalità per il vaccino NVX-CoV2373 (Novavax) in linea con i vaccini mRNA e con il vaccino Pfizer-BioNTech in particolare ”
- AstraZeneca presentava un rischio elevato di miocardite, ma solo 1/10 rispetto a Pfizer o Novavax.
- “Sarebbero necessarie ulteriori ricerche per comprendere il ruolo delle nanoparticelle nel potenziale rischio di miocardite indotta da vaccino”.
- Interpretazione: Novavax presenta un rischio di miocardite paragonabile all'mRNA di Pfizer
Dicembre 2022 Ahmad et al – Miopericardite conseguente sia a BNT162b2 che a NVX-CoV2373.
- Questo caso clinico presenta 2 casi di recidiva di pericardite e miocardite entro 1 settimana dalla vaccinazione con dose di richiamo con NVX-CoV2373
- entrambi i casi hanno presentazioni cliniche simili:
- entrambi i soggetti hanno avuto eventi mirroring in seguito alle vaccinazioni BNT162b2 e NVX-CoV2373
- Essendo individui giovani che hanno avuto reazioni entro 7 giorni da una vaccinazione senza prima dose, entrambi rientrano anche nello stesso gruppo demografico solitamente osservato nella miopericardite post-vaccino mRNA
- Entrambi soddisfano i criteri di miopericardite, con presentazione di dolore toracico pleuritico ed ECG
- Teoria:
- Miocardite di Pfizer – immunogenicità della guaina delle nanoparticelle lipidiche (LNP) necessaria per fornire l’mRNA alle cellule ospiti – causa potenziale di danno diretto alle cellule miocardiche o come altro fattore scatenante della disregolazione immunitaria.
- le nanoparticelle vengono utilizzate anche nel vaccino NVX-CoV2373, necessario per l’incorporazione della proteina S nell’ospite
7 giugno 2022 – Food and Drug Administration statunitense. Documento informativo VRBPAC sul vaccino Novavax COVID-19 (NVX-CoV2373). Aggiornato 2022.

La mia opinione…
Le buone notizie"
- Non è un vaccino mRNA contro il COVID-19
- Non ha una nanoparticella lipidica Pfizer o Moderna
- ha una quantità finita di proteine spike che si presume sia 5 ug
- Nessuna “contaminazione del DNA” (si spera)
- secondo l’azienda ha un “profilo di sicurezza accettabile”
Il cattivo
- Utilizza la proteina Spike di Wuhan
- 1:1400 morti negli studi clinici Novavax (21 decessi su 30.000 partecipanti)
- miocardite e pericardite sono ora considerati rischi identificati per NVX-CoV2373
- Ci sono stati 5 casi di miocardite/pericardite negli studi clinici Novavax, 4 erano “gravi” e ricoverati in ospedale
- L'azienda non conosce il meccanismo specifico che causa l'infiammazione del tessuto cardiaco (miocardite/pericardite)
- Lo studio di Saint-Gerons et al ha analizzato 61 casi di miocardite/pericardite segnalati agli enti regolatori, di cui il 62% uomini
- tasso di miocardite simile ai vaccini Pfizer mRNA COVID-19 (suggerendo il coinvolgimento di nanoparticelle)
- solo il 13% si è ripreso
- Documento informativo della FDA (giugno 2022)
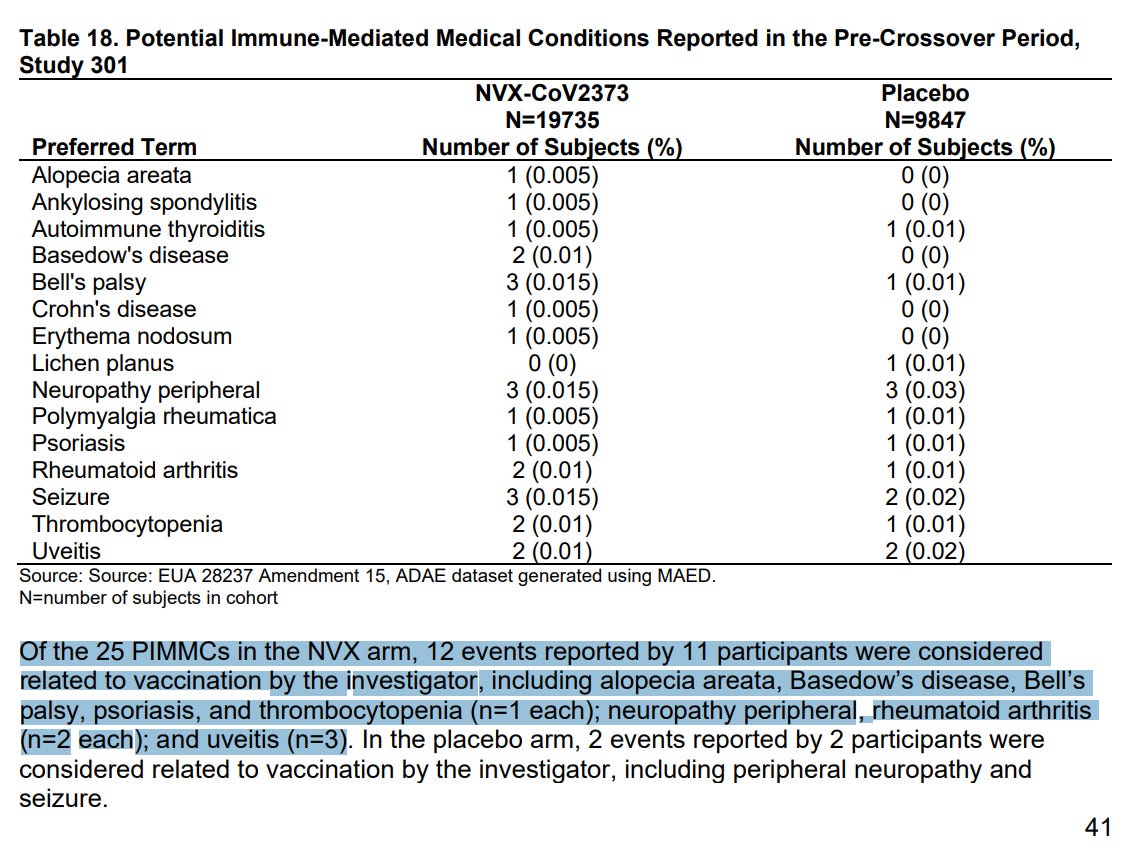
- Condizioni mediche immunomediate correlate a Novavax: alopecia, malattia autoimmune della tiroide, paralisi di Bell, psoriasi, trombocitopenia, neuropatia periferica, artrite reumatoide, uveite (tutti associati al danno alle proteine spike osservato con i vaccini mRNA dopo la distribuzione sistemica di LNP/mRNA !)
- secondo la FDA, il rischio di miocardite dopo Novavax potrebbe essere superiore rispetto ai vaccini mRNA COVID-19
Il brutto
Novavax originale non è più sul mercato negli Stati Uniti
La formulazione 2023-2024 di Novavax con la proteina spike XBB.1.5 non dispone di studi clinici che ne valutino la sicurezza o l'efficacia
- Le proteine Spike vengono miscelate in una soluzione detergente dove si “ autoassemblano ” attorno a un nucleo di Polisorbato-80
- “ Il polisorbato 80 non è un composto inerte ed è stato implicato in una serie di eventi avversi sistemici e nel sito di iniezione e infusione (ISAE)”
- contiene ANCHE un adiuvante Matrix-M a base di saponina (nanoparticelle da 40 nm, straordinariamente stabili, tenute insieme dalle interazioni saponina-colesterolo” (nei roditori provoca diminuzione del peso corporeo e della massa dei globuli rossi) – “può contribuire all’immunotossicità”
- la biodistribuzione del picco di nanoparticelle Novavax non è mai stata eseguita e l'azienda "presuppone" che rimanga "per lo più" nei linfonodi locali perché dovrebbe comportarsi come un "antigene proteico convenzionale" (NON lo è, è una nanoparticella)
- Non sono stati condotti studi per misurare la persistenza dei picchi di nanoparticelle nei tessuti locali o distali
- "Novavax prevede un basso potenziale di effetti indesiderati gravi e tossicità nei neonati, nei lattanti e nei bambini " (non lo sanno)
- "Novavax prevede un basso potenziale di effetti indesiderati gravi e tossicità nelle donne in gravidanza e nei feti " (non lo sanno)
- "Novavax non crede che esistano altre popolazioni speciali che sarebbero più suscettibili a gravi effetti indesiderati e tossicità " (non lo sanno)
Considerazioni conclusive
- Novavax è composto da 2 nanoparticelle , una rosetta di polisorbato-80/punta di Wuhan da 60 nm e Matrix-M da 40 nm (saponina-colesterolo).
- sembra che siano riusciti a farla franca non chiamando Matrix-M una nanoparticella chiamandolo invece un “adiuvante” , qualcosa che viene aggiunto per stimolare una risposta immunitaria, ma è una nanoparticella.
- Matrix-M è una nanoparticella : “L’adiuvante Matrix-M è costituito da due distinte frazioni di saponine purificate dall’albero di Quillaja saponaria Molina, combinate con colesterolo e fosfolipidi per formare nanoparticelle a gabbia aperta da 40 nm ”
- Entrambi sono realizzati in soluzioni detergenti e il nucleo in Polisorbato-80 e Matrix-M non sono inerti – entrambi potrebbero causare immunotossicità ed eventi avversi – questi rischi non sono stati studiati
- Novavax provoca miocardite paragonabile a Pfizer, solo il 13% guarisce!
- Novavax non ha mai condotto uno studio sulla biodistribuzione del picco di Polisorbato-80/Wuhan, ma è stato dimostrato che entra nel flusso sanguigno e diventa sistemico perché il documento di briefing della FDA delinea molti eventi avversi immunitari in tutto il corpo.
- Novavax inoltre non ha mai condotto studi sulla persistenza del picco nei tessuti e negli organi locali o distanti.
- Novavax – nessun dato sulla sicurezza nei neonati, lattanti e bambini
- Novavax – nessun dato sulla sicurezza in gravidanza
- L’11,4% ha avuto una reazione sistemica di grado 3+ entro 7 giorni senza dati sulla sicurezza a lungo termine.
Novavax è un vaccino a doppia nanoparticella con proteina spike tossica originale di Wuhan, con eventi avversi molto gravi (miocardite, danno immunitario sistemico), rischi potenziali molto gravi (distribuzione sistemica mai studiata di due nanoparticelle che causano danno alla proteina spike con potenziale tossicità aggiuntiva del polisorbato- 80 e Matrix-M) e troppe incognite.
Tutto questo ti sembra “sicuro”?
Avvertimento!
Nota per i lettori: fare clic sul pulsante di condivisione in alto. Seguici su Instagram e Twitter e iscriviti al nostro canale Telegram. Sentiti libero di ripubblicare e condividere ampiamente gli articoli di Global Research.
Il dottor William Makis è un medico canadese esperto in radiologia, oncologia e immunologia. Medaglia del Governatore Generale, Borsista dell'Università di Toronto. Autore di oltre 100 pubblicazioni mediche sottoposte a peer review.
L'immagine in primo piano proviene da Children's Health Defense
 La crisi mondiale del coronavirus, un colpo di stato globale contro l’umanità
La crisi mondiale del coronavirus, un colpo di stato globale contro l’umanità
di Michel Chossudovsky
Michel Chossudovsky esamina in dettaglio come questo insidioso progetto “distrugge la vita delle persone”. Fornisce un’analisi completa di tutto ciò che è necessario sapere sulla “pandemia”: dalle dimensioni mediche alle ripercussioni economiche e sociali, alle basi politiche e agli impatti mentali e psicologici.
“Il mio obiettivo come autore è quello di informare le persone in tutto il mondo e confutare la narrazione ufficiale che è stata utilizzata come giustificazione per destabilizzare il tessuto economico e sociale di interi paesi, seguita dall’imposizione del “mortale” “vaccino” COVID-19. Questa crisi colpisce l’intera umanità: quasi 8 miliardi di persone. Siamo solidali con i nostri simili e con i nostri figli in tutto il mondo. La verità è uno strumento potente”.

Nessun commento:
Posta un commento